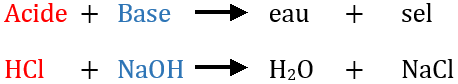
Une chimie populaire; . métaux dans la formation de sels, un métal univalent peut prendre la place de chaque atome de H, comme dans NaCl, NaN03,Na2S04; ou un métal bivalent peut prendre

Relationship between instaneous CO2 assimilation rate (A) and somatal... | Download Scientific Diagram

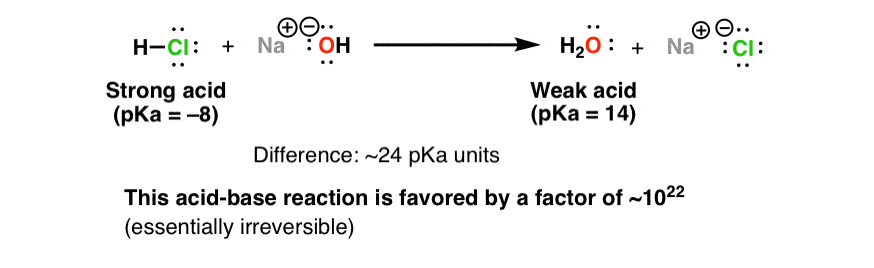
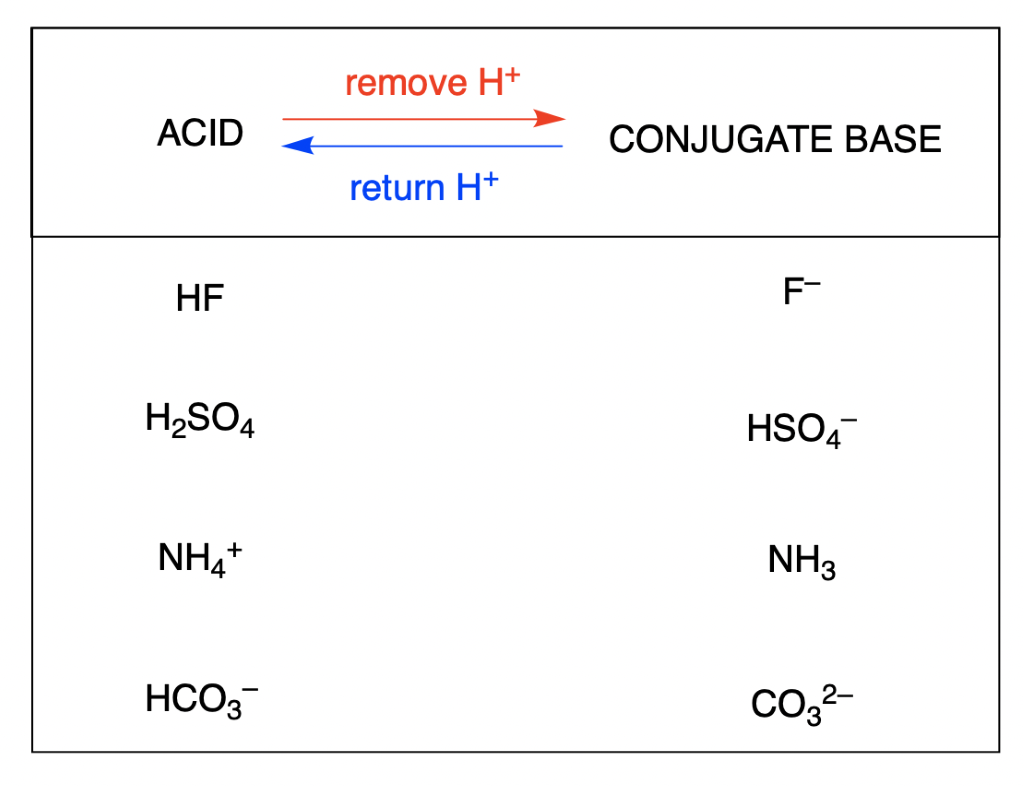
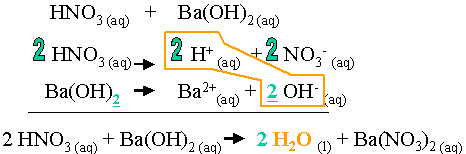
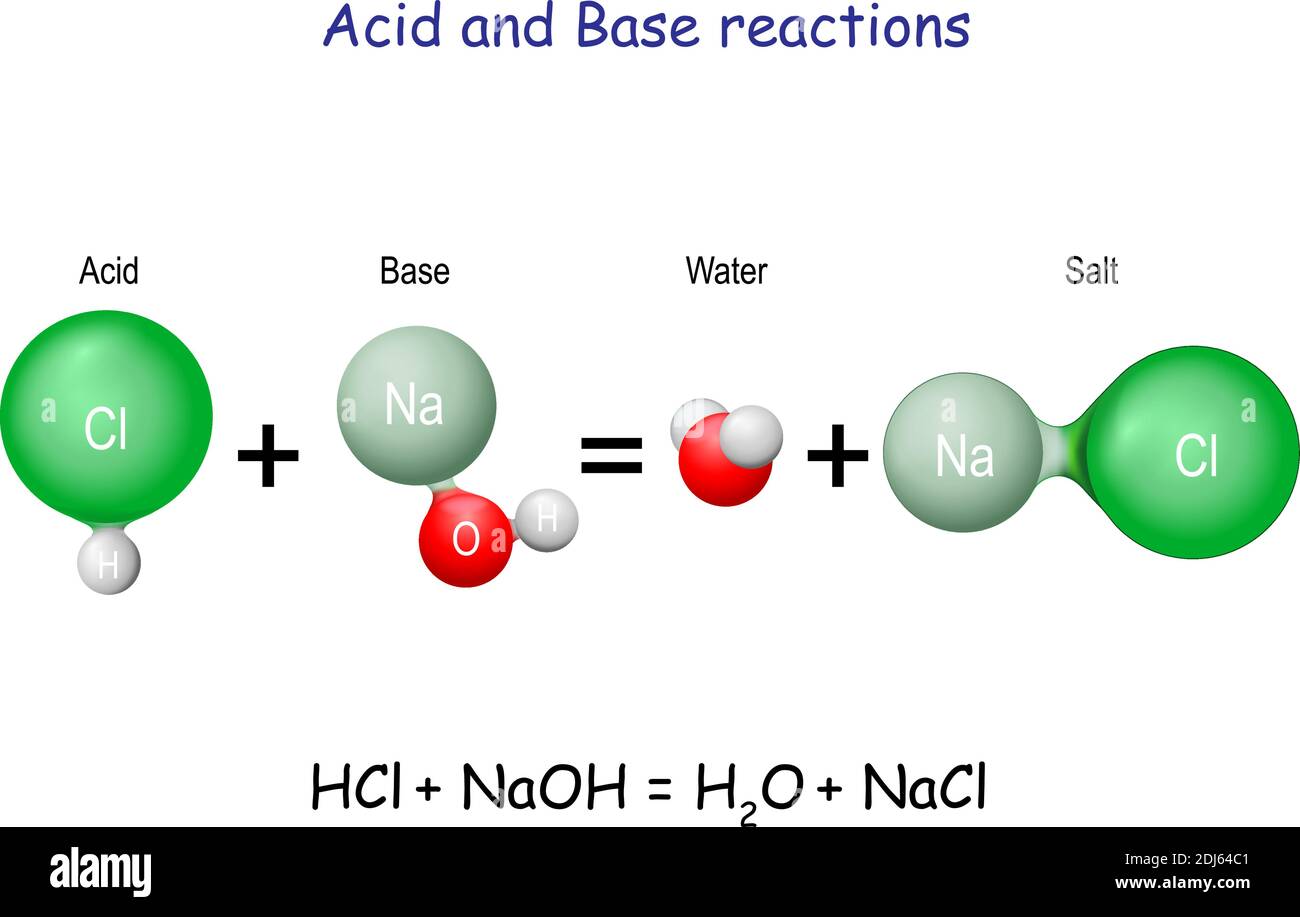
G) Sels Dans le chapitre 1, Acide + Base Sel + Eau HCl(aq) + NaOH(aq) NaCl(aq) + H2O Les sels sont des électrolytes forts qui se dissocient entièrement. - ppt video online télécharger

G) Sels Dans le chapitre 1, Acide + Base Sel + Eau HCl(aq) + NaOH(aq) NaCl(aq) + H2O Les sels sont des électrolytes forts qui se dissocient entièrement. - ppt video online télécharger

G) Sels Dans le chapitre 1, Acide + Base Sel + Eau HCl(aq) + NaOH(aq) NaCl(aq) + H2O Les sels sont des électrolytes forts qui se dissocient entièrement. - ppt video online télécharger

Réaction Acide-base. Réaction Chimique Neutralisant Les Propriétés Acides Et Basiques, Produisant Un Sel Et De L'eau. Utilisé Pour Déterminer Le Ph. Bronsted - Théorie De Lowry. Molécules De Hcl, Naoh, H2o Et

Polymers | Free Full-Text | pH and Salt Effects on the Associative Phase Separation of Oppositely Charged Polyelectrolytes

Diurnal and seasonal metabolic changes in acid-base balance of blood from human subjects living in a hot climate